Aim:
It was intended to test the biological response (poly-ADP-ribosylation of cellular proteins) of a-particles from extracellular 211At for enhanced damage to human glioblastoma cells in vitro and to discuss its suitability for potential application in therapy of high-grade gliomas.
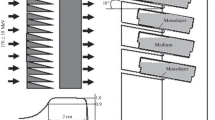
Materials and Methods: Confluent cultures of human glioblastoma cells were exposed to different doses of a-radiations from homogeneously distributed extracellular 211At. Cellular poly-ADP-ribosylation of all proteins including histones was monitored since it is an indirect but sensitive indicator of chromatin damage and putative repair in both normal and malignant mammalian cells.
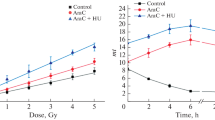
Results: A significant diminution (average 85.6%) in poly-ADP-ribosylation of total cellular proteins relative to that for non-irradiated glioblastoma cells was observed following 0.025 to 1.0 Gy a-radiations. In the dose range of 0.0025 to 0.01 Gy there was an increase with a maximum value of approximately 119.0% at 0.0025 Gy. Below 0.0025 Gy no change in poly-ADP-ribosylation was observed.
Conclusions: Level of cellular poly-ADP-ribosylation of proteins at 0.025 to 1.0 Gy of a-radiation dose from 211At appears to cause enhanced damage by creating molecular conditions which are not conducive to repair of DNA damages in human glioblastoma cells in vitro. Therefore, it is assumed that clinical application of 211At at least in this dose range might enhance clinical efficacy in radiotherapy of cancer.
Ziel:
Es war die Absicht, die biologische Reaktion (Poly-ADP-Ribosylierung zellulärer Proteine) menschlicher Glioblastomzellen in vitro auf verstärkte Schadensbildung durch a-Teilchen von extrazellulärem 211At zu testen und deren Berücksichtigung für eine potentielle Anwendung in der Therapie von malignen Glioblastomen zu diskutieren.
Material und Methode: Konfluente Kulturen menschlicher Glioblastomzellen wurden unterschiedlichen a-Dosen von homogen verteiltem extrazellulärem 211At ausgesetzt. Die zelluläre Poly-ADP-Ribosylierung aller Proteine, einschließlich die der Histone, wurde bestimmt, da sie ein indirekter, aber empfindlicher Indikator für Chromatinschäden und mutmaßlich für die Reparatur in normalen und entarteten Zellen ist.
Ergebnisse: Eine signifikante Verringerung (durchschnittlich 85,6%) der Poly-ADP-Ribosylierung aller zellulären Proteine, relativ zu der der nichtbestrahlten Glioblastomzellen, wurde nach 0,025 bis 1,0 Gy a-Bestrahlung beobachtet. Im Dosisbereich von 0,0025 bis 0,01 Gy gab es einen Anstieg mit einem maximalen Wert von angenähert 119% bei 0,0025 Gy. Unterhalb von 0,0025 Gy wurde keine Änderung der Poly-ADP-Ribosylierung beobachtet.
Schlußfolgerung: Das Niveau poly-ADP-ribosylierter Proteine im 211At-a-Dosisbereich von 0,025 bis 1,0 Gy scheint eine erhöhte Schädigung dadurch zu bewirken, daß molekulare Bedingungen geschaffen werden, die der Reparatur von DNA-Schäden in menschlichen Glioblastomzellen in vitro nicht förderlich sind. Daher wird angenommen, daß die klinische Anwendung von 211AT – zumindest in diesem Dosisbereich – die Wirksamkeit der Radiotherapie von Krebs steigern könnte.
Similar content being viewed by others
Author information
Authors and Affiliations
Additional information
Submitted: 23 Feb 1999. Accepted: 16 June 1999.
Rights and permissions
About this article
Cite this article
Schneeweiss, F., Sharan, R. & Brown, I. 211At-αDose Dependence of Poly-ADP-Ribosylation of Human Glioblastoma Cells in Vitro Suitability in Cancer Therapy?. Strahlenther Onkol 175, 458–461 (1999). https://doi.org/10.1007/s000660050036
Published:
Issue Date:
DOI: https://doi.org/10.1007/s000660050036